Conteúdo da página
ToggleAtualmente, o Brasil tem duas vacinas contra o SARS-CoV-2 aprovadas para uso emergencial: a Coronavac, desenvolvida pela empresa chinesa Sinovac, e a AstraZeneca/Oxford, produzida pela Universidade de Oxford em parceria com a multinacional inglesa.
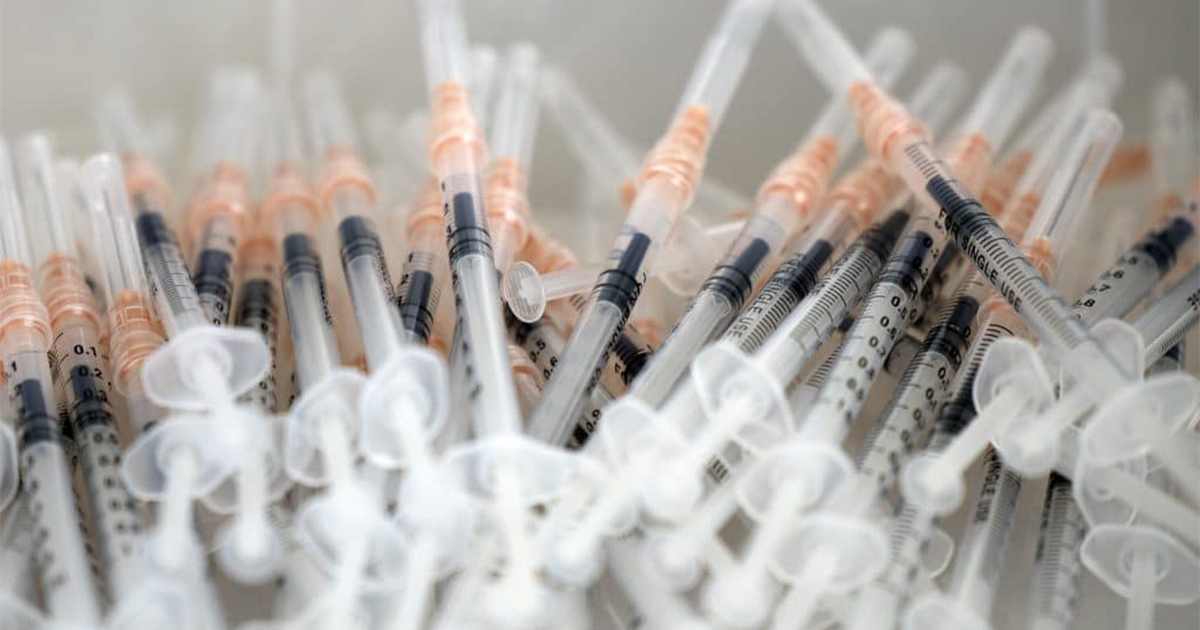
Para que um imunizante seja aprovado e esteja disponível no mercado, são necessários de 10 a 15 anos de muita pesquisa e vários testes. A aprovação para uso emergencial das duas vacinas disponíveis foi feita em tempo recorde, mas ainda é possível que os imunizantes passem por melhorias.
Autoridades, médicos e cientistas ressaltam a importância de termos um produto brasileiro com tecnologia 100% nacional, mesmo que isso demore anos. As razões vão desde a preocupação de que a Covid-19 se torne uma doença sazonal até a dependência de importação de insumos, processo que atrasa a fabricação de vacinas no País.
A USP é uma das instituições que assumiram o compromisso de desenvolver uma vacina do zero. São sete projetos em andamento nos vários campi da Universidade.
A vacina em spray nasal do Instituto do Coração (Incor) da Faculdade de Medicina (FMUSP); a vacina nanoparticulada da Faculdade de Medicina de Ribeirão Preto (FMRP); a vacina vetorizada da Faculdade de Zootecnia e Engenharia de Alimentos (FZEA); as quatro plataformas vacinais em ensaios pré-clínicos do Instituto de Ciências Biomédicas (ICB): a nanovacina, a vacina de subunidades, e as vacinas de DNA e de RNA.
As duas primeiras são as que se encontram em fase avançada. O grupo que desenvolve a vacina em spray nasal deve iniciar os testes toxicológicos em breve. Já a nanoparticulada, da FMRP, aguarda a aprovação da Agência Nacional de Vigilância Sanitária (Anvisa) para iniciar os ensaios clínicos de fase 1 e 2.
O Jornal da USP conversou com os líderes dessas pesquisas e, nesta reportagem, explica todos os detalhes.

PxHere
A USP é uma das instituições que assumiram o compromisso de desenvolver uma vacina do zero.
Vacinas em desenvolvimento na USP
| UNIDADE DA USP EM QUE ESTÁ ALOCADA | PROJETO | FASE EM QUE SE ENCONTRA | INVESTIMENTO ATÉ 02/2021 |
|---|---|---|---|
| Instituto do Coração (Incor) | spray nasal | finalizando os ensaios pré-clínicos | MCTI – R$ 20 milhões; Fapesp – R$ 5 milhões; USP Vida – R$ 104 mil |
| Faculdade de Medicina de Ribeirão Preto (FMRP) | vacina nanoparticulada | aguardando autorização da Anvisa para iniciar os testes clínicos |
Não divulgado |
| Faculdade de Zootecnia e Engenharia de Alimentos (FZEA) |
vacina de vetor viral | ensaios pré-clínicos | CNPq/MCTI – R$ 4.334.600,00 |
| Instituto de Ciências Biomédicas (ICB) | vacina de subunidades nanovacina vacina de DNA Vacina de RNA |
ensaios pré-clínicos ensaios pré-clínicos ensaios pré-clínicos ensaios pré-clínicos |
MCTI – R$ 1,1 milhão; Fapesp – R$ 200 mil |
Spray nasal: a vacina sem dor
A ideia de uma vacina contra a Covid-19 indolor, bem aceita por crianças, gestantes e idosos, desenvolvida com tecnologia nacional e que ataca o vírus na porta de entrada para o organismo, pode virar uma realidade em breve. A produção do imunizante em formato de spray nasal começou em abril de 2020 e, atualmente, é liderada por Jorge Kalil Filho, diretor do Laboratório de Imunologia do Instituto do Coração (Incor) do Hospital das Clínicas (HC) da Faculdade de Medicina (FMUSP).
Em entrevista ao Jornal da USP no Ar 1ª Edição, o médico disse que a proposta do trabalho, desde o início, era estudar melhor a resposta imune contra o coronavírus para criar uma vacina baseada nos alvos da resposta imune mais eficientes.
 Jorge Kalil Filho Fonte: Curriculum Lates“Tem duas formas de nós combatermos o vírus: não deixando ele entrar em uma célula, ou se ele entrou na célula e a infectou, ele pode ser morto por uma outra célula do sistema imune”, explica Kalil Filho. Para o estudo, então, coletou-se o sangue de pessoas contaminadas com o vírus e foi possível analisar os alvos da resposta de anticorpos e também da resposta celular. Essa investigação mais profunda do antígeno é o que diferencia a nova vacina das demais.
Jorge Kalil Filho Fonte: Curriculum Lates“Tem duas formas de nós combatermos o vírus: não deixando ele entrar em uma célula, ou se ele entrou na célula e a infectou, ele pode ser morto por uma outra célula do sistema imune”, explica Kalil Filho. Para o estudo, então, coletou-se o sangue de pessoas contaminadas com o vírus e foi possível analisar os alvos da resposta de anticorpos e também da resposta celular. Essa investigação mais profunda do antígeno é o que diferencia a nova vacina das demais.
“A prova de conceito e a formulação da vacina estão prontas e os dados serão publicadas em breve”, afirma Marco Antonio Stephano, pesquisador da Faculdade de Ciências Farmacêuticas (FCF) da USP e um dos criadores do projeto.
“Devemos partir agora para os testes toxicológicos, que fazem parte dos ensaios pré-clínicos.”
Nessa fase, os pesquisadores devem avaliar a segurança da vacina em camundongos e porcos. De acordo com Stephano, os suínos não são suscetíveis ao vírus, mas neles será possível avaliar, além da produção de anticorpos, a resposta celular. “Conseguiremos, também, testar o dispositivo para inoculação no nariz, que será usado em seres humanos.”
Resposta imune celular ocorre quando os linfócitos ou células T atacam o microrganismo que está dentro da célula, eliminando as células infectadas. Também sinalizam para outras células do sistema imune, além de gerar imunidade celular.
Se aprovada, o próximo passo é pedir a liberação da Agência Nacional de Vigilância Sanitária (Anvisa) para iniciar os ensaios clínicos de fase 1 e 2.
Além do Incor e da Faculdade de Ciências Farmacêuticas, fazem parte do projeto o Instituto de Ciências Biomédicas (ICB) e o Instituto de Química (IQ), ambos da USP, além de cientistas da Universidade Federal de São Paulo (Unifesp) e da Universidade Estadual de Campinas (Unicamp).
A principal fonte de recursos vem da Rede Vírus, do Ministério da Ciência, Tecnologia e Inovações (MCTI), da Fundação de Amparo à Pesquisa do Estado de São Paulo (Fapesp), além do auxílio do Projeto USP Vida.
O imunizante já prevê a proteção contra as novas variantes em circulação: a africana, a de Manaus e a inglesa.
 Foto: 8photo via freepik
Foto: 8photo via freepik
Vacina nanoparticulada
Com diversas plataformas tecnológicas de vacinas já desenvolvidas e conhecimento adquirido ao longo de mais de 30 anos de trabalho com imunizantes, Célio Lopes Silva, professor do Departamento de Bioquímica e Imunologia da Faculdade de Medicina de Ribeirão Preto (FMRP) da USP e coordenador do Laboratório de Vacinas Gênicas da FMRP, decidiu enviar um projeto ao Ministério da Ciência, Tecnologia e Inovações (MCTI) assim que a pandemia foi declarada.
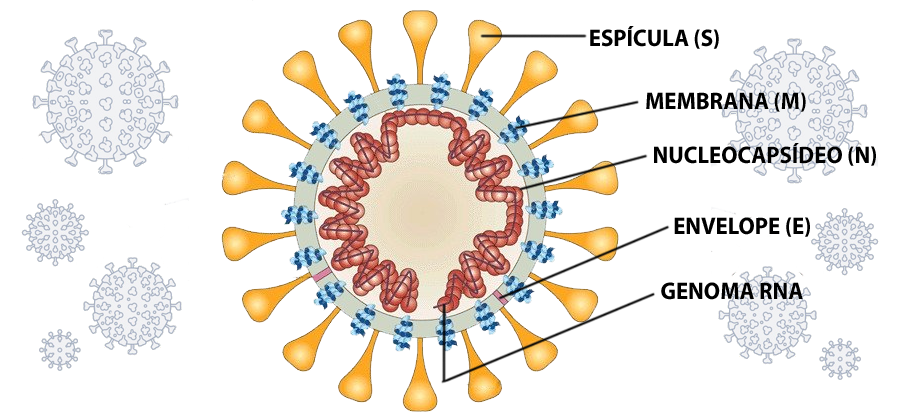
A ideia inicial era produzir uma proteína recombinante a partir das proteínas S, do núcleo do capsídeo e da membrana (ver figura abaixo). Por meio de análises de bioinformática, os pesquisadores criaram um antígeno e tentaram expressar aquelas proteínas em culturas de bactérias e em baculovírus (vírus de insetos utilizados no controle biológico de pragas agrícolas e também como ferramenta para expressão de diferentes proteínas, inclusive de antígenos virais), mas o resultado foi insatisfatório.
Lopes montou uma nova estratégia e fez testes com três tipos de proteínas: a S, a S1 e o RBD (da sigla receptor-binding domain, é um receptor localizado dentro da unidade S1 da proteína S que identifica a célula humana) e, nos testes de imunogenecidade, a S1 como um todo foi mais eficiente.
“Os resultados mostraram que ela é mais imunogênica, ou seja, estimula a produção de anticorpos e neutraliza a entrada do vírus na célula”, comemora o professor.
Para que o antígeno chegue até a célula humana e ative o sistema imune, ele precisa ser conjugado a um carreador e, nesse caso, foi usado um lipídeo desenvolvido por uma empresa estadunidense. Como conta o professor Silva, o produto já foi testado com sucesso em outros tipos de vacina.
“Além de carrear o antígeno, o produto é imunomodulador, ou seja, estimula a produção de interferon 1, as primeiras células de defesa estimuladas quando o organismo é atacado por um patógeno. O SARS-CoV-2 desativa o sistema de produção de interferons, por isso, ter esse carreador no nosso produto traz mais essa vantagem”, explica Silva ao Jornal da USP.
Os resultados dos ensaios pré-clínicos, segundo o pesquisador, são animadores. Os testes prévios de eficácia mostraram que a vacina protegeu os animais infectados. Agora, está em andamento o teste de toxicidade.
“Enviamos um dossiê com informações de protocolo dos testes e seus resultados para a Anvisa em 15 de fevereiro.” Após a primeira análise da agência, o documento retorna à FMRP para ajustes e, daí, será reenviado à agência regulatória. Nessa etapa, a USP pedirá autorização para iniciar os testes clínicos de fase 1 e 2.
“No geral, podemos definir essa como uma vacina nanoparticulada, que contém o antígeno S1, veiculada com um carreador. É um imunizante que, ao entrar na célula, estimula o sistema imune inato (interferons tipo 1, ativação de macrófagos, etc.), produz citocinas que facilitam o processo de estimulação do sistema imune, além de estimular a produção de linfócitos B (que impedem a entrada do vírus na célula) e de linfócitos T do tipo CD4+ e CD8+”, resume Silva.
A Faculdade de Medicina de Ribeirão Preto firmou parcerias com a Farmacore, startup responsável pelo desenvolvimento do antígeno, e a PDS Biotecnology, que fornece o carreador.
Silva não divulga os valores já investidos, mas os recursos são provenientes do Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq), da Farmacore Biotecnologia Ltda. e da americana PDS Biotechnology.
Esquema da proteína S do SARS-CoV-2
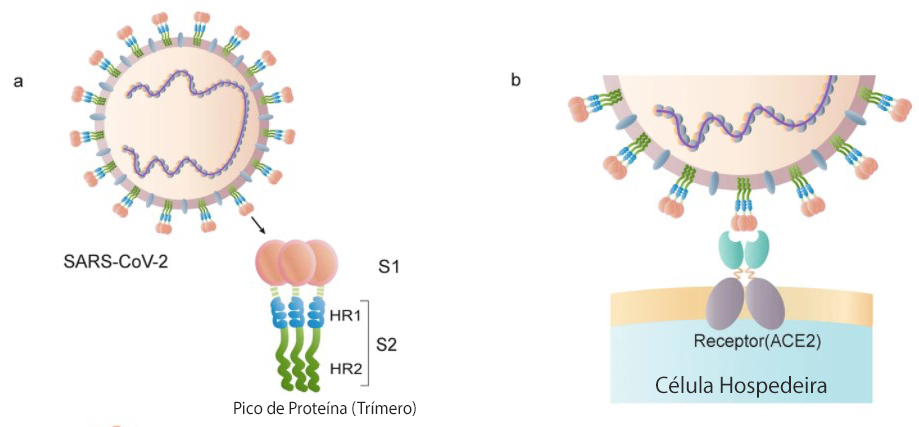
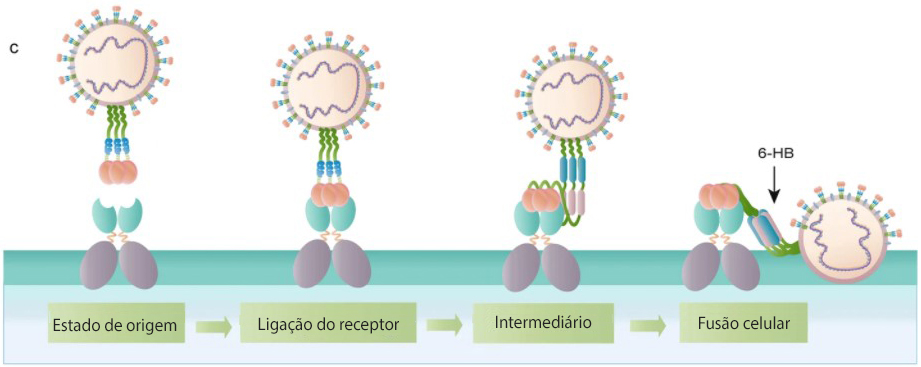
a A estrutura esquemática da proteína S. b A proteína S liga-se ao receptor ACE2. c O processo de ligação e fusão vírus-célula mediado pela proteína S. d O ciclo de vida do SARS-CoV-2 nas células hospedeiras.
Estrutura da proteína SARS-CoV-2 S
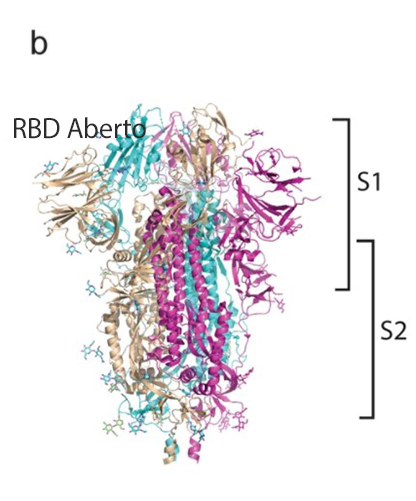
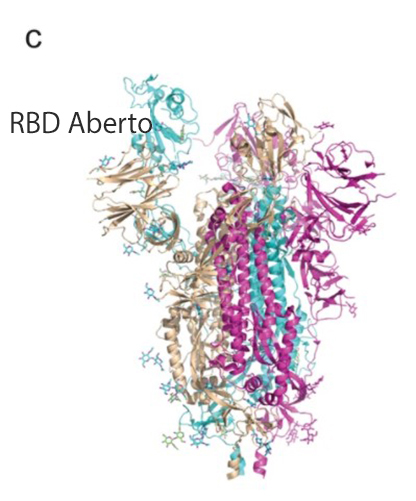
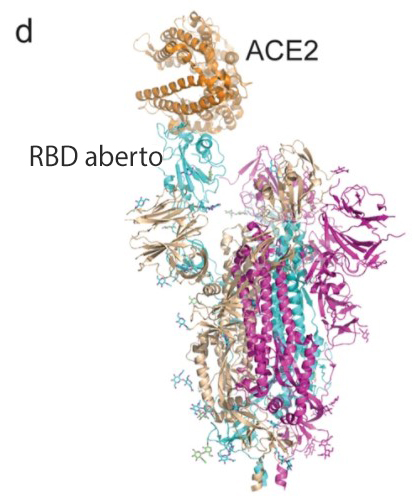
A RBD é um dos alvos estudados para desenvolver a vacina contra a covid-19. As figuras b – c mostram o RBD da proteína S com status fechado e aberto. d A proteína S liga-se a ACE2 com RBD aberto na subunidade S1. e a estrutura de seis hélices formada por HR1 e HR2 da subunidade S2.
Fonte: Nature
Vacina de vetor viral
A ideia de se produzir uma vacina vetorizada contra o SARS-CoV-2 surgiu da própria expertise do laboratório de Heidge Fukumasu, médico veterinário e professor da Faculdade de Zootecnia e Engenharia de Alimentos (FZEA) da USP, em Pirassununga. Até o início da pandemia, Fukumasu trabalhava no desenvolvimento de vacinas para tratar diversos tipos de câncer em animais. Com o aumento dos casos de Covid-19, Fukumasu propôs a criação de uma força-tarefa para realizar testes de RT-PCR para diagnóstico da doença na população da região de Pirassununga.
O envio de um projeto para o CNPq, cuja proposta era trabalhar na produção de uma vacina para a Covid-19 – na mesma plataforma utilizada para o desenvolvimento de imunizantes contra o câncer em animais -, foi consequência de todo esse processo.
Ainda em fase inicial, o grupo trabalha para criar um imunizante para humanos e gatos, pois esses animais também são suscetíveis à doença. Por meio de engenharia genética, são feitas modificações nas proteínas do SARS-CoV-2 que precisam ser expressas e o material é adicionado ao vírus vacinal da doença de Newcastle (patologia altamente contagiosa que infecta aves domésticas e selvagens). Depois, esse antígeno é inserido em ovo de galinha galado, para que ele cresça e se reproduza. “O vírus de Newcastle se reproduz muito bem em galinhas e isso pode nos ajudar em uma outra etapa”, afirma Fukumasu ao Jornal da USP.
O Instituto Butantan tem a planta de produção de vacina contra a influenza, que também é baseada em ovos. “Essa plataforma funciona durante seis meses no ano para produzir o imunizante. Nos seis meses restantes, poderíamos utilizá-la para produzir o nosso imunizante”, explica o médico veterinário.
De acordo com pesquisador, há duas maneiras de aproveitar o vírus na criação de uma vacina. Se usá-lo vivo, há a estimulação do sistema imune para produzir anticorpos e gerar resposta celularinativado, haverá essencialmente a produção de anticorpos.
Fazem parte do estudo Helena Fereira e Fabiana Bressen, da FZEA. Parcerias foram estabelecidas com Paulo Lee Hoo, do Instituto Butantan, e Qingzhong Yu, do Departamento de Agricultura dos Estados Unidos.
Até agora, foram investidos R$ 334.600,00, recursos esses vindos do CNPq/MCTI.
Um laboratório, diferentes abordagens
“A nossa ideia é produzir diferentes plataformas vacinais, ou seja, a tecnologia que será empregada na produção de um imunizante.” É assim que Luis Carlos Ferreira, diretor do Insituto de Ciências Biomédicas (ICB) da USP e coordenador do Laboratório de Desenvolvimento de Vacinas resume a missão do trabalho a que se propôs.
A estratégia principal do grupo liderado por Ferreira é trabalhar com partes do vírus, ou seja, as proteínas que o compõem – e em diferentes formulações -, seja o material genético dele em formatos distintos.
Os recursos (R$ 1 milhão e 300 mil) são provenientes da Fundação de Amparo à Pesquisa do Estado de São Paulo (Fapesp) e do Ministério da Ciência, Tecnologia e Inovações (MCTI).
Ao todo, são quatro projetos de desenvolvimento de vacinas contra a covid-19, e todos eles estão na fase de avaliação de imunogenicidade em modelo animal (camundongos). A partir de março, se tudo correr como planejado, serão iniciados ensaios de proteção em camundongos suscetíveis ao vírus.
O trabalho, feito em parceira com outros grupos de pesquisa da Universidade, possui características próprias. Veja a relação logo abaixo.
Vacinas de subunidades
Nessa plataforma, os pesquisadores trabalham com fragmentos do SARS-CoV-2 (proteínas spike e do nucleocapsídeo, por exemplo) e utilizam a bactéria Escherichia coli para replicar as proteínas que serão utilizadas para desenvolver a vacina. “Funciona como uma minifábrica”, explica Marianna Favaro, bióloga e uma das pesquisadoras líderes do projeto no ICB.
Os cientistas testaram essa abordagem, chegaram até os ensaios pré-clínicos, mas os resultados não animaram o grupo. “Vimos que a vacina induzia a uma boa produção de anticorpos, mas eles não eram neutralizantes, ou seja, não impediam a entrada do vírus na célula dos animais”, relata a pesquisadora.
Por isso, Marianna e os demais envolvidos no projeto estão fazendo uma readaptação tecnológica para que outro tipo de produção seja empregada. A ideia é substituir bactérias por células humanas. “Só de subunidades testamos 11 construções diferentes, em vias distintas. Foi um trabalho bem amplo, mas encontramos esse gargalo que era maior do que a formulação em si”, conclui.
Nanovacinas
Marianna foi a responsável por desenvolver uma tecnologia em que a proteína do vírus é modificada geneticamente e passa a se comportar como uma nanopartícula, que mimetiza as características de tamanho e carga virais. Seria um fragmento do vírus (que pode ser a proteína spike ou a do nucleocapsídeo) e, por meio de interações químicas, as pontas dessa proteína se unem e adquirem a forma de um disco. “Ao invés de termos somente a proteína avulsa com um adjuvante (medicamento que reforça a ação de outro), ela adquire uma formato tridimensional, mimetizando a atuação do patógeno”, explica a pesquisadora.
A próxima etapa consiste em iniciar os ensaios pré-clínicos de imunogenicidade e inocular a vacina em animais, para depois se pensar em testes em humanos.
Vacinas gênicas
Depois que as vacinas da BioNTech/Pfizer e da Moderna foram aprovadas para uso nos Estados Unidos e na Europa, o termo “vacinas gênicas” ganhou mais notoriedade. Esses dois tipos de imunizantes utilizam moléculas de DNA e RNA sintetizados em laboratório e, quando injetadas, são absorvidas pelas células, que interpretam as informações e passam a produzir proteínas do vírus. O sistema imunológico é, então, ativado porque entende que existem partículas estranhas no organismo.
“As vacinas gênicas são muito vantajosas em relação às outras vacinas porque elas não usam o vírus propriamente dito”, explica Jamile Ramos da Silva, microbiologista e líder da produção de vacinas de RNA no ICB. “Usamos o próprio organismo humano para produzir proteína do vírus que queremos combater. Além disso, elas são produzidas muito mais rápido que os imunizantes convencionais.”
Vacina de DNA
O objetivo principal do grupo envolvido nesse projeto é produzir uma vacina que induza à produção de linfócitos TCD8+ específicos para o SARS-CoV-2 e destrua as células infectadas. Na primeira fase de desenvolvimento, os cientistas decidiram fazer a análise proteômica do vírus (investigação do conjunto de proteínas e suas isoformas expressas em uma amostra biológica) para identificar os epitopos (sítio de ligação específico que é reconhecido por um anticorpo ou por um receptor de superfície de um linfócito T) possivelmente imunogênicos. Depois, os dados foram cruzados com os HLAs mais frequentes na população brasileira.
HLA são genes que apresentam grande variedade entre as pessoas, marcam de forma única cada célula e definem precisamente quem e o que somos biologicamente. Estão localizados na superfície de quase todas as células humanas e são os responsáveis por apresentar um “invasor” do nosso corpo às células de defesa, os leucócitos. Alguns subtipos estão relacionados à suscetibilidade a certas doenças e são os principais responsáveis por rejeitar um órgão ou um tecido transplantado.
Como explica Rubens Prince, biomédico do ICB e participante do estudo, cada célula T tem um tipo específico de HLA, que pode variar de acordo com a etnia de uma população e a genética individual . “E por isso ser muito diverso no mundo, nós selecionamos os oito HLAs mais frequentes”, explica o pesquisador. “Com isso, as chances desses epitopos induzirem a uma resposta específica para a população brasileira são grandes.”
Vacina de RNA
Todas as vacinas de DNA que tiveram sucesso nos testes em laboratório do ICB foram redirecionadas para a abordagem na forma de RNA, inclusive aquela desenvolvida com base no sistema imunológico da população brasileira. A afirmação é de Jamile Ramos, pesquisadora do LDV que está à frente do trabalho. Jamile passou um ano na Universidade da Pensilvânia (EUA) aprendendo e trabalhando no laboratório que desenvolveu a tecnologia aplicada nas vacinas da Moderna e da Pfizer.
Jamile contou ao Jornal da USP que umas das frentes em desenvolvimento prevê utilizar a plataforma de RNA para desenvolver nanovacinas. “Substituiremos a produção de imunizantes de subunidades em bactérias por uma construção via RNA”, explica. “Será a fusão de duas inovações bem importantes. Se funcionar, a vacina será alvo tanto de uma patente como de um produto inédito.”
Apesar de ser uma plataforma que dá maior agilidade à produção de um imunizante, a vacina de RNA apresenta algumas desvantagens em relação à de DNA. “O RNA é mais instável, fácil de ser degradado, por isso precisamos envolvê-lo em uma capa de gordura para que ele chegue até as células humanas”, detalha a pesquisadora. “Mas se seguirmos todos os protocolos, ela é altamente imunogênica, consegue gerar resposta de linfócitos e de anticorpos. Com essas novas variantes circulando aqui no Brasil, podemos rapidamente mudar a sequência genética e obter uma formulação que combata essas mutações.”
OS DIFERENTES TIPOS DE VACINA
Existem três abordagens principais para projetar uma vacina. As diferenças específicas são o uso de um vírus ou bactéria inteiros; apenas as partes do microrganismo que ativam o sistema imunológico; ou apenas o material genético que fornece as instruções para fazer proteínas específicas e não o vírus inteiro.

Utiliza um vírus ou bactérias inteiras
Usa apenas os fragmentos que induzem a uma resposta do sistema imunológico
Utiliza apenas o material genético
Vacina de subunidade
É aquela que usa apenas as partes muito específicas – as subunidades – de um vírus ou bactéria que o sistema imunológico precisa reconhecer. Ele não contém o microrganismo inteiro nem usa um vírus seguro como vetor. As subunidades podem ser proteínas ou açúcares. A maioria das vacinas do calendário infantil são vacinas de subunidade, protegendo as pessoas de doenças como coqueluche, tétano, difteria e meningite meningocócica.
Vacina inativada
A primeira maneira de fazer uma vacina é pegar o vírus ou bactéria causador da doença, ou um muito semelhante a ele, e inativá-lo usando produtos químicos, calor ou radiação. Vacinas contra a gripe e a pólio são produzidas com esse tipo de abordagem e podem ser fabricadas em grande escala.
A desvantagem é que a produção necessita de instalações laboratoriais especiais para cultivar o vírus ou bactéria com segurança, pode ter um tempo de produção relativamente longo e provavelmente exigirá duas ou três doses para serem administradas.
Vacina atenuada
Usa uma versão viva, mas enfraquecida, do vírus ou uma versão muito semelhante. A vacina contra sarampo, caxumba e rubéola, e a vacina contra varicela e herpes zoster são exemplos desse tipo de vacina. Esta abordagem usa tecnologia semelhante à vacina inativada e pode ser fabricada em grande escala. No entanto, vacinas como esta podem não ser adequadas para pessoas com sistema imunológico comprometido.
Vacina de vetor viral
Esse tipo de vacina utiliza um vírus não patogênico, como um adenovírus, que não causa nenhuma doença ou prejuízos à saúde. O adenovírus é modificado geneticamente e passa a carregar dentro de si as instruções para a produção de uma proteína característica da doença que se quer imunizar. Ao entrar nas células, o adenovírus faz com que elas passem a produzir essa proteína e, a partir daí, o sistema imunológico reconhece esse corpo estranho e cria formas para combatê-lo. A vacina do ebola é uma imunizante de vetor viral.
Vacina gênica
Essa é uma vacina que fornece um conjunto específico de instruções às nossas células para que façam a proteína específica do patógeno que queremos combater.
Antes da pandemia de covid-19, não havia nenhuma vacina genética aprovada para uso em humanos, embora algumas delas para tratar certos tipos de câncer estivessem passando por testes clínicos. Por causa da pandemia, a pesquisa nessa área progrediu muito rápido e algumas vacinas de mRNA para covid-19 já receberam autorização para uso emergencial, como as da Moderna e da Pfizer/BioNTech.
Moléculas de DNA e RNA são as instruções que nossas células usam para produzir proteínas específicas

DNA
transcrição
RNA
Fonte: Organização Mundial da Saúde
As opiniões expressas nesse artigo não refletem, necessariamente, a opinião da Diálogos do Sul
Veja também
Se você chegou até aqui é porque valoriza o conteúdo jornalístico e de qualidade.
A Diálogos do Sul é herdeira virtual da Revista Cadernos do Terceiro Mundo. Como defensores deste legado, todos os nossos conteúdos se pautam pela mesma ética e qualidade de produção jornalística.
Você pode apoiar a revista Diálogos do Sul de diversas formas. Veja como:
- Cartão de crédito no Catarse: acesse aqui
- Boleto: acesse aqui
- Assinatura pelo Paypal: acesse aqui
- Transferência bancária
Nova Sociedade
Banco Itaú
Agência – 0713
Conta Corrente – 24192-5
CNPJ: 58726829/0001-56
Por favor, enviar o comprovante para o e-mail: assinaturas@websul.org.br - Receba nossa newsletter semanal com o resumo da semana: acesse aqui
- Acompanhe nossas redes sociais:
YouTube
Twitter
Facebook
Instagram
WhatsApp
Telegram